除ATP外,其他一些重要的活化载体分子也参与氧化还原反应,并且通常是细胞内偶联反应的一部分。这些活化载体专门用于携带处于高能级的电子(有时称为“高能电子”)和氢原子。其中最重要的电子载体是 NAD⁺(烟酰胺腺嘌呤二核苷酸)以及与之密切相关的 NADP⁺(烟酰胺腺嘌呤二核苷酸磷酸)。
在酶催化反应中,当底物分子被氧化时,每个分子都会接受一“能量包”,对应两个电子和一个质子(H⁺),从而分别转化为 NADH(还原型烟酰胺腺嘌呤二核苷酸)和 NADPH(还原型烟酰胺腺嘌呤二核苷酸磷酸)(见图 2–36)。因此,这些分子可以被视为氢离子(H⁺加两个电子,或 H⁻)的载体。
像 ATP 一样,NADPH 是一种活化载体,参与许多重要的生物合成反应,否则这些反应在能量上是不利的。
NADPH 的生成。
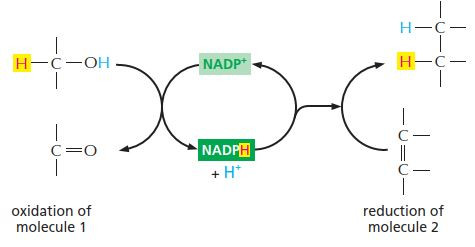
《Molecular Biology of the Cell》7E Figure 2–36 A
在一系列特殊的放能分解代谢反应中,从底物分子上移除两个氢原子。两个电子和其中一个氢原子(即氢化离子 H⁻)加到 NADP⁺ 的烟酰胺环上形成 NADPH;第二个氢原子作为质子(H⁺)释放到溶液中。这是典型的氧化还原反应,其中底物被氧化,而 NADP⁺ 被还原。
NADPH 在随后的氧化还原反应中容易释放所携带的氢化离子,因为烟酰胺环在没有它时能够达到更稳定的电子排布。在这个后续反应中,NADPH 被氧化,而底物被还原。NADPH 能够有效地将氢化离子转移给其他分子,原因与 ATP 易于转移磷酸类似:在两种情况下,转移都会伴随较大的负自由能变化。
NADPH 上额外的磷酸基团对 NADPH 的电子转移特性没有影响,因为它远离参与电子转移的区域。然而,它确实使 NADPH 分子的形状略有不同于 NADH,从而使 NADPH 和 NADH 能够作为底物结合到完全不同的酶集合。因此,这两类载体用于在两组不同的分子之间转移电子(或氢化离子)。
为什么会有这种分工呢?答案在于需要独立调控两组电子转移反应。NADPH 主要与催化合成代谢反应的酶协同作用,为合成高能生物分子提供高能电子。相比之下,NADH 在通过氧化食物分子生成 ATP 的分解代谢系统中具有特殊作用。NADH 由 NAD⁺ 生成,NADPH 由 NADP⁺ 生成,它们通过不同途径并独立调控,以便细胞可以根据两种截然不同的需求调节电子供应。在细胞内,NAD⁺ 与 NADH 的比例保持较高,而 NADP⁺ 与 NADPH 的比例保持较低。这为 NAD⁺ 提供了充足的氧化剂,为 NADPH 提供了充足的还原剂,以满足它们在分解代谢和合成代谢中的特殊作用。